Die HÄRTE des WASSERS
Die
überwiegende Mehrheit aller Aquarien wird, von wenigen Ausnahmen abgesehen, mit
Leitungswasser gefüllt, das aus Grundwasser oder Wasser aus Fließgewässern,
das ebenfalls dem Grundwasser entstammt, gewonnen wird. Grundwasser ist
letztendlich irgendwann einmal gefallenes Niederschlagswasser, das bis in tiefe
Boden und Untergrundschichten gesickert
ist. Die Härte des Wassers wird dabei dadurch verursacht, dass das CO2-haltige
(durch Kontakt mit der Atmosphäre) Niederschlagswasser auf seinem Weg durch
verschiedene Erd- und Gesteinsschichten Mineralien aus diesen Schichten herauslöst.
Je nachdem, durch welche Gesteinsschichten das Wasser nun fließt, bis es sich
als Grundwasser auf einer wasserundurchlässigen Schicht sammelt, und wie lange
es dort verweilt, ergibt sich eine unterschiedliche Härte im Wasser. Siehe Abb.
1.
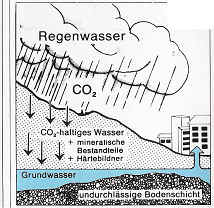
Unser Leitungswasser verdient als Lebenselement der Zierfische und Pflanzen eine besondere Beachtung. Als CO2-haltiges Niederschlagswasser dringt es in die Erdschichten ein und nimmt hier viele Mineralien auf.
Unter "Härte" eines Wassers versteht man seinen Gehalt an Erdalkali-Ionen.
Dabei unterscheidet man:
Gesamthärte
(GH):
Summe aller im Wasser gelösten Erdalkali-Ionen, d. h. Calcium- und Magnesium-Ionen. Andere, seltener vorkommende Ionen werden dabei nicht berücksichtigt. Die Menge an Ca2+ - und Mg2+ -Ionen wird in die entsprechende Menge an Calciumoxid CaO umgerechnet. Dabei entsprechen 10mg CaO in 100 mL Wasser einem Grad deutscher Härte (1 °dH)
Die oben erwähnten Calcium- und Magnesium-Ionen liegen im Wasser nicht als reine Ionen, sondern als gelöste Salze, z.B. Calcium- oder Magnesiumkarbonat, -sulfat oder -chlorid vor. Die Menge an Erdalkali-Ionen, die nun als Karbonat vorliegt, bezeichnet man als Karbonathärte. Gewöhnlich ist die KH niedriger als die GH. In manchen Fällen, z. B. in einigen Gewässern SüdostAsiens, kann es vorkommen, dass alle Calcium- und Magnesium-Ionen als Karbonate und darüber hinaus auch noch andere Ionen, z. B. Natrium oder Kalium, ebenfalls als Karbonate gelöst vorliegen, wodurch man KH größer als GH findet. Ein einfaches Schema soll dies veranschaulichen.
Gemessen wird in Deutschland in Grad deutscher Härte °dH.
Als erstrebenswert gilt eine Karbonathärte zwischen 5 und 15°dH und eine Gesamthärte bis etwa 20° dH.
|
unter 7 °dH |
weiches Wasser |
|
7-14 °dH |
mittelhartes Wasser |
|
14-21 °dH |
hartes Wasser |
|
über 21 °dH |
sehr hartes Wasser |
Dies soll jedoch nicht heißen, dass nicht auch bei höherer Härte Pflanzen und Fische gut gepflegt werden können, wenn alle anderen Wasserwerte möglichst optimal gehalten werden. Bei Fischen sollte man beachten, dass Eier und Jungfische weniger anpassungsfähig sind als die ausgewachsenen Tiere. Bei der Zucht empfiehlt es sich deshalb, die in der Literatur für die einzelnen Arten angegebenen Wasserwerte einzuhalten.